在感染 SARS-CoV-2 后,部分 COVID-19 患者会表现出中枢神经系统和/或外周神经系统功能障碍的症状,其中最常见的包括嗅觉丧失、味觉障碍和头痛,此外还有脑雾、嗜睡和抑郁等。在一项大型回顾性队列研究中,感染 SARS-CoV-2 后 6 个月表现出神经疾病的发生风险增加。然而,SARS-CoV-2 对神经元的感染性仍存在争议。
2024 年 1 月 17 日,来自美国康奈尔医学院的陈水冰课题组联合多个团队在 Cell Stem Cell 杂志上发表了一项研究 SARS-CoV-2 infection causes dopaminergic neuron senescence,通过人多能干细胞(hPSCs)诱导的多巴胺神经元,证实 SARS-CoV-2 可以感染大脑中的多巴胺(DA)神经元并引发细胞衰老,发出引起炎症的化学信号。研究团队通过高通量筛选,发现三种已获 FDA 批准的药物——利鲁唑(治疗肌萎缩侧索硬化症)、二甲双胍(治疗糖尿病)和伊马替尼(治疗癌症)——可以阻断 SARS-CoV-2 感染进而阻止多巴胺神经元衰老。

图片来源:Cell Stem Cell
研究内容
hPSC 来源的多巴胺神经元易受 SARS-CoV-2 感染
研究人员使用带有报告基因的 hPSC 分化而成的多巴胺神经元来验证其对 SARS-CoV-2 的易感性,结果显示暴露于 SARS-CoV-2 的多巴胺神经元中约为 5% 被感染。此外,他们还通过透射电镜检测到 SARS-CoV-2 感染的 hPSC 来源的纯化多巴胺能神经元中存在病毒颗粒。阻断 ACE2 抗体在低感染量和高感染量条件下均能防止病毒感染,表明 SARS-CoV-2 感染 hPSC 来源的多巴胺能神经元依赖于与 ACE2 受体的相互作用。
为了进一步验证 hPSC 来源的多巴胺能神经元对 SARS-CoV-2 感染的易感性,研究人员从人类胚胎干细胞系 MEL-1 和一个帕金森病对照组(PD-control)诱导的多能干细胞系(相当于健康对照)中分化出多巴胺能神经元。RT-qPCR 和免疫染色研究结果都证实了从 MEL-1 hESCs 分化出的多巴胺能神经元和 PD-control iPSCs 都对 SARS-CoV-2 具有易感性并支持其复制。
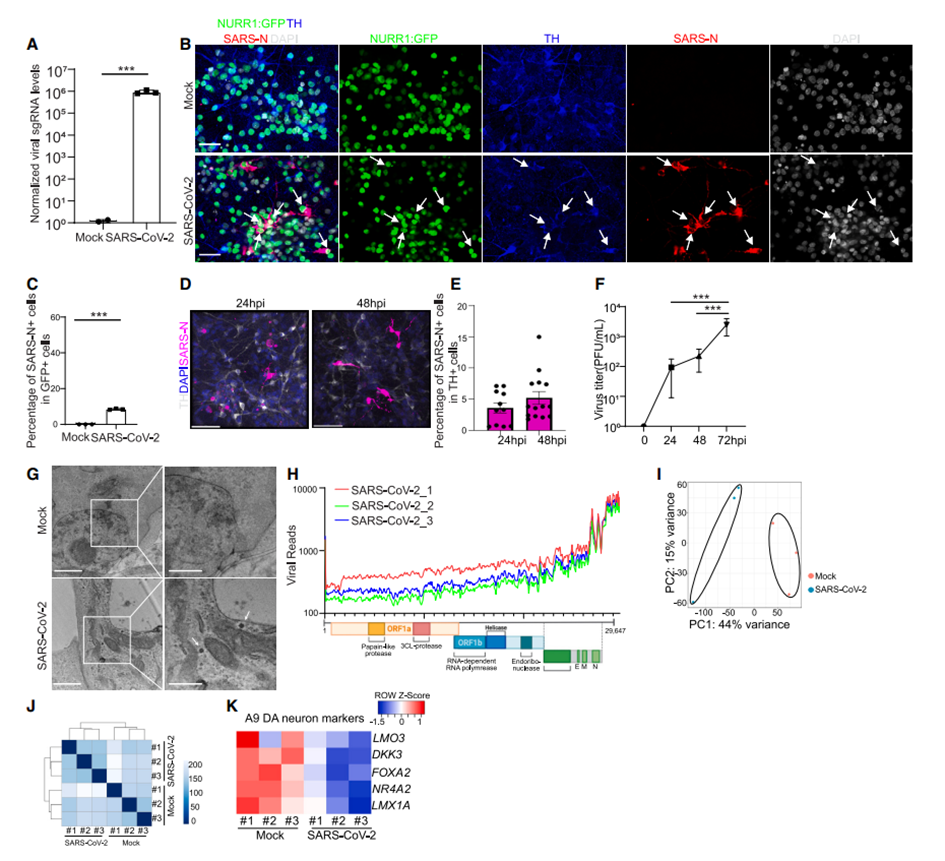
图片来源:Cell Stem Cell
SARS-CoV-2 感染可诱导多巴胺神经元衰老
在对 SARS-CoV-2 感染的 hpsc 来源的 DA 神经元和对照组之间差异表达基因的独创性通路分析表明,细胞周期、DNA 复制和衰老通路是 SARS-CoV-2 感染的 DA 神经元中上调最多的通路。基因集富集分析进一步证实了 SARS-CoV-2 感染的 DA 神经元中衰老通路的富集。通过 RNA-seq 数据进一步分析,发现在 SARS-CoV-2 感染的 DA 神经元中,趋化因子/细胞因子转录物和炎症相关基因的上调,衰老相关基因也显著上调。与此形成鲜明对比的是,衰老通路在 SARS-CoV-2 感染的肺类器官、胰腺细胞、肝类器官和心肌细胞中未显著富集。
衰老细胞的一个关键特征是衰老相关分泌表型(SASP)的激活。在 SARS-CoV-2 感染后的 DA 神经元中,SASP 相关基因(包括 CCL2、CCL20、CSF1、CXCL11、GDF15、IGF2R、IL1B、IL6ST、IQGAP1 和 TNFRSF11B)表达上调;细胞衰老的生物标志物 SA-β-gal(衰老相关的 β-半乳糖苷酶)活性也上调。透射电镜在 SARS-CoV-2 感染的 DA 神经元中检测到脂褐素,这是 DA 神经元的另一种衰老相关标志物。此外,SARS-CoV2 感染的 DA 神经元细胞核大小也增加。RT-qPCR 分析显示 IGFBP7 上调和 LMNB1 下调,这些基因被报道与多巴胺神经元衰老相关。总之,多种证据证明了 SARS-CoV-2 感染可诱导多巴胺神经元衰老。
高通量筛选以识别阻断 SARS-CoV-2 诱导的多巴胺能神经元衰老的候选药物
为了找到可能保护多巴胺能神经元免受 SARS-CoV-2 诱导的衰老的候选药物,研究人员使用已获 FDA 批准的药物库进行了高通量筛选。在药物处理后 6 小时,H9 hPSC 来源的多巴胺能神经元感染 SARS-CoV-2,并在 72 小时后分析 β-gal 活性,并对初筛药物进行了不同浓度下的效力和细胞毒性评估。
最终,他们发现三种药物以剂量依赖方降低了 β-gal 活性,而不引起细胞毒性。这三种药物为利鲁唑(治疗肌萎缩侧索硬化症)、二甲双胍(治疗糖尿病)和伊马替尼(治疗癌症)。
用 10 mM 利鲁唑、50 mM 二甲双胍或 10 mM 伊马替尼处理的多巴胺能神经元与 DMSO 处理组相比,显示出 β-gal+细胞的百分比显著减少。RT-qPCR 分析显示这三种药物均减少了与衰老途径相关的基因 IGFBP7 的表达,并上调了 LMNB1 的表达。此外,与 DMSO 处理的细胞相比,这三种药物还减少了溶酶体积累。RNA-seq 分析结果显示,与感染对照组相比,在利鲁唑、二甲双胍和伊马替尼处理的感染 SARS-CoV-2 的 DA 神经元中,SASP 表型的基因和衰老途径的基因均下调。
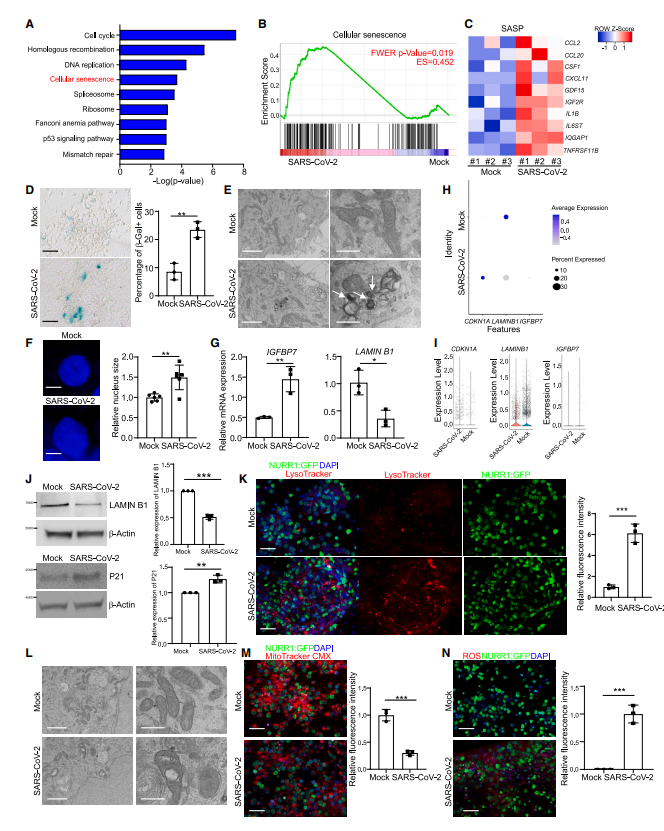
图片来源:Cell Stem Cell
利鲁唑、二甲双胍和伊马替尼通过阻断 SARS-CoV-2 感染来阻止 DA 神经元衰老
药物可能通过阻断 SARS-CoV-2 感染,或是通过直接干预衰老途径实现减缓衰老。为了区分这两种可能性,研究人员使用 DA 神经元用 10 mM 利鲁唑、50 mM 二甲双胍或 10 mM 伊马替尼处理(预处理),然后感染 SARS-CoV-2。在 48 小时后,RT-qPCR 分析表明,利鲁唑、二甲双胍和伊马替尼都减少了病毒 RNA,这一结果通过针对 SARS-CoV-2 核衣壳蛋白的免疫染色得到了进一步证实。
为了确定药物候选物的治疗潜力,他们先用 SARS-CoV-2 感染了 DA 神经元,然后在感染后 4 小时用 10 mM 利鲁唑、50 mM 二甲双胍或 10 mM 伊马替尼处理(后处理)。与预处理一致,在后处理试验中,候选药物同样显著减少了病毒 RNA。此外,这三种药物候选物还在 MEL-1 来源的 DA 神经元中阻断了病毒感染。综上所述,这些结果表明利鲁唑、二甲双胍和伊马替尼通过阻断 SARS-CoV-2 感染阻止了 DA 神经元的衰老。
接着,研究人员进一步研究了这三种药物抗病毒活性的分子机制。
基于先前的研究报道,伊马替尼能够通过结合 ACE2 受体阻断肺器官样体中的 SARS-CoV-2 病毒入侵。在感染 SARS-CoV-2-entry 病毒后进行的 luciferase 活性分析显示,较对照组相比,在伊马替尼处理条件下感染后的 DA 神经元的 luciferase 活性减少,表明伊马替尼可以阻断 SARS-CoV-2 病毒进入 DA 神经元。
基因集富集分析确定了利鲁唑处理条件下脂肪酸生物合成途径的下调。一些研究已经表明脂肪酸生物合成在 SARS-CoV-2 感染中发挥重要作用,这表明利鲁唑可能通过抑制脂肪酸生物合成来阻断 SARS-CoV-2 感染。基因集富集分析还确定了在二甲双胍处理条件下 AMPK 途径的上调。近期已有研究确定了二甲双胍作为潜在的 COVID-19 治疗药物,并将增加的 AMPK 信号与对 SARS-CoV-2 的保护性联系起来。
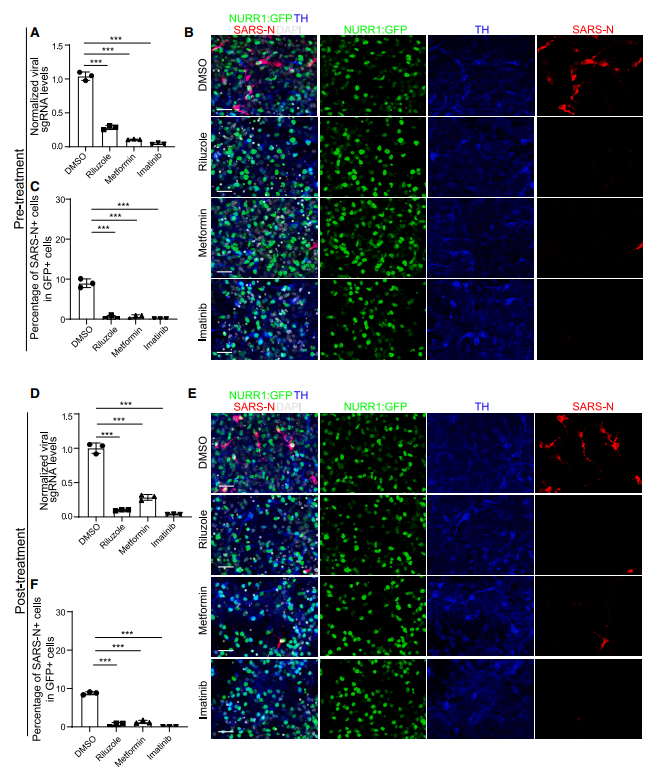
图片来源:Cell Stem Cell
此外,他们还研究了感染病毒的患者的尸检样本,以证实他们对实验室培养细胞的观察结果。研究团队在 COVID-19 患者的人类黑质组织中发现了炎症和细胞衰老的特征以及低水平的 SARS-CoV-2 转录物。
总结
综上所述,该研究发现人类多能干细胞(hPSCs)诱导的多巴胺神经元易受 SARS-CoV-2 感染,并在感染后会引发炎症和细胞衰老反应。通过高通量筛选,研究团队确定了三种已被 FDA 批准的药物(利鲁唑、二甲双胍和伊马替尼)可以通过阻止 SARS-CoV-2 感染拯救细胞衰老表型。
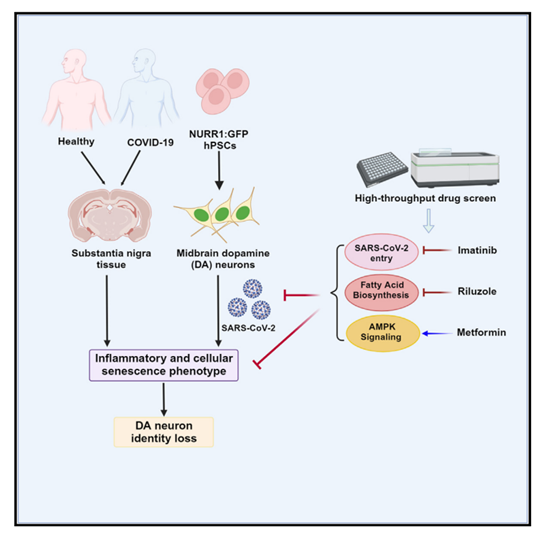
图片来源:Cell Stem Cell
该研究的通讯作者陈水冰教授表示:「这个项目最初是为了研究不同器官中各种类型的细胞如何对 SARS-CoV-2 感染做出反应。我们测试了肺细胞、心脏细胞、胰腺 β 细胞,但衰老途径仅在多巴胺神经元中被激活。这是一个完全出乎意料的结果。」
研究人员认为,对这一发现的进一步研究可能会揭示与长期 COVID 相关的神经系统症状。此外,由于多巴胺神经元衰老是帕金森病的标志之一,研究人员建议应监测长期 COVID 患者发生帕金森病相关症状的风险。
参考资料:Liuliu Yang et al, SARS-CoV-2 infection causes dopaminergic neuron senescence, Cell Stem Cell (2024). DOI: 10.1016/j.stem.2023.12.012













